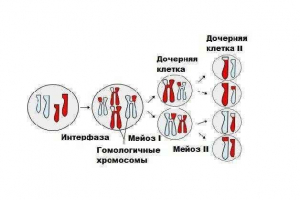
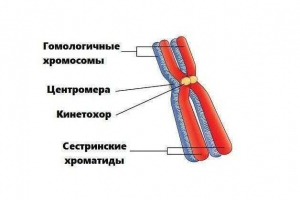
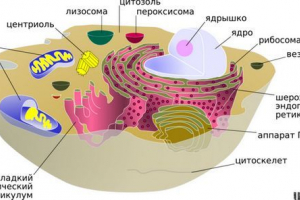
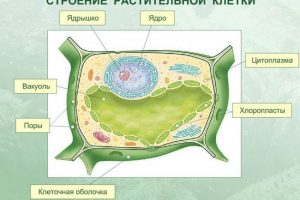
Hemijski sastav ćelija
Sadržaj

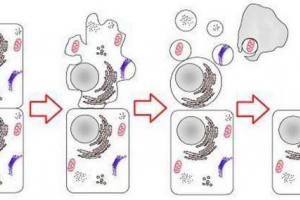
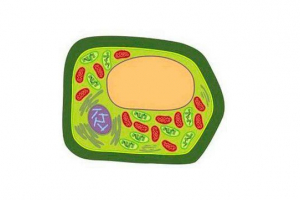
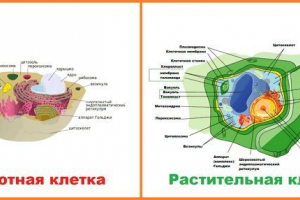
Ćelija - Osnovna jedinica života na zemlji. Ima sve znakove živi organizma: raste, množi se, razmjene sa okruženjima i energijom, reagira na vanjske podražaje. Početak biološke evolucije povezan je sa pojavom mobilnih oblika života na zemlji. Jednoćelijski organizmi su postojeći ćelije odvojeno jedna od druge. Tijelo svih višećelijskih - životinja i biljaka - izgrađeno od više ili više ćelija koje su vrste blokova koji čine složeni organizam. Bez obzira da li je ćelija holistički živi sistem - poseban organizam ili je samo dio toga, obdaren je skupom značajki i svojstava zajedničkim za sve ćelije.
Hemijski sastav ćelija

Oko 60 elemenata periodične mendeleev periodične, koje se nalaze u neživoj prirodi, pronađeni su u ćelijama. Ovo je jedan od dokaza zajednice žive i nežive prirode. U živim organizmima najčešći su vodonik, kiseonik, ugljik i nitrogen, koji čine oko 98% mase ćelija. To je zbog osobina hemijskih svojstava vodonika, kisika, ugljika i azota, kao rezultat toga što su se pokazali najprikladnijim za formiranje molekula koji obavljaju biološke funkcije. Ova četiri elementa su sposobna da formiraju vrlo jake kovalentne obveznice uparivanjem elektrona koji pripadaju dva atoma. Kovalentno povezani ugljični atomi mogu formirati okvire bezbrojnih mnogo različitih organskih molekula. Budući da se ugljeni atomi lako formiraju kovalentne obveznice sa kisikom, vodonik, azotom, kao i sumpor, organski molekuli dostižu izuzetnu složenost i razne strukture.
Pored četiri glavna elementa u ćeliji u primjetnim količinama (10y i 100y kamatni postotak) su sadržani gvožđe, kalijum, natrijum, kalcijum, magnezijum, hlor, fosfor i sumpor. Svi ostali elementi (cink, bakar, jod, fluor, kobalt, mangan i itd.) su u kavezu u vrlo malim količinama i zato se nazivaju elementima u tragovima.
Hemijski elementi su dio anorganskih i organskih spojeva. Inorganski spojevi uključuju vodu, mineralne soli, ugljični dioksid, kiselinu i bazu. Organske veze su Proteini, Nukleinske kiseline, Ugljikohidrati, Debeo (lipidi) i Lipoidi.
Neki proteini sadrže sumpor. Dio nukleinskih kiselina je fosfor. Molekula hemoglobina uključuje gvožđe, magnezijum sudjeluje u izgradnji molekule hlorofill. Mikroelementi, uprkos izuzetno niskom sadržaju u živim organizmima, igraju važnu ulogu u procesima života. Jod Uključeno u hormon štitne žlijezde - Thyroxine, kobalt - u sastavu vitamina u12Hormon otoka dijela gušterače - insulin - sadrži cink. U neku ribu mjesto gvožđe u molekulama pigmenata koji nose kisik zauzima bakar.
Anorganske tvari

Voda
N2O - najčešća veza u živim organizmima. Njegov sadržaj u različitim ćelijama fluktuira u prilično širokim granicama: od 10% u caklinu zuba do 98% u tijelu meduze, ali iznosi oko 80% tjelesne težine. Izuzetno važna uloga vode u osiguravanju procesa života zbog svojih fizikohemijskih svojstava. Polaritet molekula i sposobnosti formiranja vodikovih veza čine vodu dobrom otapalom za ogromnu količinu tvari. Većina hemijskih reakcija javlja se u ćeliji može se pojaviti samo u vodenoj otopini. Voda sudjeluje u mnogim hemijskim transformacijama.
Ukupni broj vodonika između molekula vode varira ovisno o t°. Sa T° Taljenje leda uništava otprilike 15% vodikovih obveznica, na ° 40 ° C - pola. Prilikom prebacivanja u gasovito stanje, sve vodikove veze su uništene. To objašnjava visoku specifičnu toplinsku sposobnost vode. S promjenom t ° vanjskog okruženja, voda apsorbuje ili ističe toplinu zbog pauze ili novog formiranja vodikovih veza. Na ovaj način fluktuirajući T ° u ćelijama su manji nego u okolini. Visoka vrućina isparavanja u osnovi efektivnog mehanizma za prijenos topline u biljkama i životinjama.
Voda kao otapala sudjeluje u pojavu osmoze koja igra važnu ulogu u životu tela. Osmoza se naziva prodorom molekula otapala kroz polupropusnu membranu u rješenje bilo koje tvari. Semipermermeri se nazivaju membrane koje preskoče molekule otapala, ali nestaju molekuli (ili ioni) rastvorene supstance. Shodno tome, osmoza je jednostrana difuzija molekula vode u smjeru otopine.
Mineralne soli

Većina neorganskih B-u ćelijama je u obliku soli u disociranom ili u čvrstom stanju. Koncentracija kationa i anija u ćeliji i u okruženju koja okružuje. Ćelija sadrži prilično puno i puno na. U vanselularnim medijima, na primjer, u krvnoj plazmi, u morskoj vodi, naprotiv, puno natrijuma i malog kalijuma. Navodnjava ćelije ovisi o omjeru koncentracija na iona na ionama+, K+, Ca2+, Mg2+. U tkivima multikelularnih životinja K je dio višeikelijske supstance koja pruža kvačilo ćelije i naručivu lokaciju. Osmotski pritisak u ćeliji i njezina svojstva međuspremnika ovise o koncentraciji soli. Buloff je sposobnost ćelije da održava slabo poznatu reakciju svojih sadržaja na stalnom nivou. Buffernost unutar ćelije uglavnom pružaju ioni2Ro4 i NRA42-. U vanselularnim tečnostima i u krvi igra se uloga međuspremnika2Tako3 i NSO3-. Anioni vezuju ioni H i hidroksidni ioni (on-), tako da se reakcija unutar ćelije vanćelijske tečnosti praktično ne mijenja. Neaktivne mineralne soli (na primjer, fosfor CA) osigurava snagu kostiju kralježnjaka i mollusk sudopera.
Ćelije organske ćelije
Proteini
Među organskim tvarima ćelije proteina nalaze se u prvom mjestu u broju (10 - 12% ukupne mase ćelije) i vrijednosti. Proteini su visoki molekularni pojmovi za molekularne težine (s molekularne težine od 6000 do milion. i više) čiji su monomeri aminokiseline. Živi organizmi koriste 20 aminokiselina, iako ima mnogo više. Sastav bilo koje aminokiseline uključuje Amino grupu (-NH2), ima osnovna svojstva i karboksilna grupa (-son) sa kiselim svojstvima. Dvije aminokiseline povezane su u jednoj molekuli uspostavljanjem HN-CO komunikacije sa izdanje molekule vode. Odnos između amino grupe jedne aminokiseline i karboksila je još jedan zvan peptid. Proteini su polipeptidi koji sadrže desetine i stotine aminokiselina. Molekuli različitih proteina razlikuju se jedan od drugog s molekularne težine, brojem, sastavom aminokiselina i slijedom njihove lokacije u polipeptidnom lancu. Jasno je da se proteini odlikuju ogromnom sortom, njihov broj svih vrsta živih organizama procjenjuje se na broj 10deset - deset12.
Lanac aminokiselinskih jedinica povezanih kovalentnim peptidnim vezama u određenom redoslijedu naziva se primarna struktura proteina. U ćelijama, proteini imaju pogled na spiralne upletene vlakne ili kuglice (globule). To je zbog činjenice da je u prirodnom proteinu, lanac polipeptida postavljen strogo na određeni način, ovisno o hemijskoj strukturi aminokiselina uključenih u njegov sastav.

U početku se lanac polipeptida pretvara u spiralu. Postoji atrakcija između atoma susjednih okreta i formiranih vodikovih obveznica, posebno između NH- i grupa smještenih na susjednim okretama. Aminokisenski lanac, uvijen u obliku spirale formira sekundarnu strukturu proteina. Kao rezultat daljnjeg polaganja spirale, dođe do konfiguracije specifične za svaki protein, nazvan tercijarna struktura. Tercijarna struktura nastala je zbog djelovanja spojnih snaga između hidrofobnih radikala dostupnih u nekim aminokiselinama i kovalentnim obveznicama između cistein aminokiselina SH grupa (S-S-komunikacija). Broj aminokiselina sa hidrofobnim radikalima i cisteinom, kao i redoslijedom njihove lokacije u polipeptidnom lancu specifični su za svaki protein. Shodno tome, osobitosti tercijarne strukture proteina određene su njenom primarnom strukturom. Biološka aktivnost proteinskih eksponata samo u obliku tercijarne strukture. Stoga zamjena čak i jedna aminokiselina u polipeptidnom lancu može dovesti do promjene konfiguracije proteina i smanjenja ili gubitka svoje biološke aktivnosti.
U nekim se slučajevima molekuli proteina kombiniraju jedni s drugima i mogu obavljati svoju funkciju samo u obliku kompleksa. Dakle, hemoglobin je kompleks četiri molekula i samo u takvom obliku može se priložiti i prevoziti. Takvi agregati su rezanirana struktura proteina. U pogledu njegovog sastava, proteini su podijeljeni u dvije glavne klase - jednostavne i složene. Jednostavni proteini sastoje se samo od nukleinskih kiselina aminokiselina (nukleotida), lipida (lipoproteina), IU (metaloproteides), p (fosfoproproproods).
Funkcije proteina u ćeliji su izuzetno raznolike. Jedna od najvažnijih - građevinskih funkcija: proteini su uključeni u formiranje svih ćelijskih membrana i ćelija ćelije, kao i unutarćelijske strukture. Enzimska (katalitička) uloga proteina je izuzetno važna. Enzimi ubrzavaju hemijske reakcije u ćeliji, u 10ki i 100n Milion puta. Funkcija motora pruža posebni kontraktilni proteini. Ovi proteini su uključeni u sve vrste pokreta na koje su ćelije i organizmi sposobni: treperenje cilija i premlaćivanje ukusa iz najjednostavnijeg, skraćenice mišića kod životinja, kretanje lišća u biljkama, itd. Transportna funkcija proteina je pričvrstiti hemijske elemente (na primjer, hemoglobin pridruži se) ili biološki aktivne tvari (hormone) i prenose ih u tkiva i tijela tijela. Zaštitna funkcija izražava se u obliku razvoja posebnih proteina zvanih antitijela, kao odgovor na prodor u tijelo vanzemaljskih proteina ili stanica. Antitela veže i neutraliziraju vanzemaljske tvari. Proteini igraju važnu ulogu kao izvore energije. Sa punim dijeljenjem 1g. Proteini se ističu 17,6 kJ (~ 4.2 kcal).
Ugljikohidrati

Ugljikohidrati ili saharidi - organske tvari sa općom formulom (CH2O)N. U većini ugljikohidrata, broj atoma H atoma veći je od broja atoma o tome, kao u molekulama vode. Stoga su te supstance nazivene ugljikohidratima. U dnevnom kavezu ugljikohidrati su u količinama koji ne prelaze 1-2, ponekad 5% (u jetri, u mišićima). Najbogatije u ugljikohidratima biljne ćelije, gdje njihov sadržaj dostiže u nekim slučajevima 90% mase suve tvari (sjemenke, gomolje krumpira itd.D.).
Ugljikohidrati su jednostavni i složeni. Jednostavni ugljikohidrati nazivaju se monosaharidi. Ovisno o broju atoma ugljikohidrata u molekuli monosaharide, oni se nazivaju trijanovima, tetroze, patosama ili hekse. Od šest ugljičnih monosaharida - hexose - glukoza, fruktoza i galaktoza najvažnija je važnost. Glukoza se nalazi u krvi (0,1-0,12%). Penoze riboze i deoksiriboze dio su nukleinskih kiselina i ATP-a. Ako se dva monosaharida kombiniraju u jednoj molekuli, takva se veza naziva Disaharidom. Šećer hrane dobiven iz trske ili šećerne repe sastoji se od jedne molekule glukoze i jedna molekula fruktoze, mliječnog šećera - od glukoze i galaktoze.
Kompleksni ugljikohidrate formirani mnogim monosaharidima nazivaju se polisaharidi. Monomer takvih polisaharida, poput škroba, glikogena, celuloze, je glukoza. Ugljikohidrati obavljaju dvije glavne funkcije: izgradnju i energiju. Celuloza formira zidove biljnih ćelija. Sofisticirani polisaharidni hitin služi kao glavna strukturalna komponenta vanjskog kostura artropoda. Funkcija izgradnje Chitina izvodi gljive. Carbohidrati igraju ulogu glavnog izvora energije u ćeliji. U procesu oksidacije 1 g. Ugljikohidrati objavljeni 17,6 kJ (~ 4.2 kcal). Škrob u biljkama i glikogenu kod životinja deponiran je u ćelijama i poslužuju kao energetski rezervat.
Nukleinske kiseline

Vrijednost nukleinskih kiselina u ćeliji je vrlo velika. Značajke njihove kemijske strukture pružaju mogućnost skladištenja, prenosa i prijenosa nasljedstvo dječijim ćelijama informacija o strukturi proteinskih molekula, koji se sintetizira u svakom tkivu u određenoj fazi pojedinog razvoja. Budući da su većina svojstava i znakova ćelija zbog proteina, jasno je da je stabilnost nukleinskih kiselina najvažnija uvjet za normalan život ćelija i čitavih organizama. Bilo kakve promjene u strukturi ćelija ili aktivnosti fizioloških procesa u njima, utječu na vitalnu aktivnost. Studija strukture nukleinskih kiselina izuzetno je važna za razumijevanje nasljeđivanja karakteristika organizama i obrasca funkcioniranja, obje pojedinačne ćelije i mobilne sustave - tkiva i organe.
Postoje dvije vrste nukleinskih kiselina - DNK i RNA. DNK - polimer koji se sastoji od dvije nukleotidne spirale, zatvorenika tako da se formira dvostruka spirala. Molekuli DNK Monekuli su nukleotidovi koji se sastoje od azotske baze (adenina, timina, guanina ili citozin), ugljikohidrata (deoksirilo) i ostataka fosforne kiseline. Azotyst baze u molekuli DNK međusobno su povezani različitim brojem N-veza i nalaze se u parov: adenin (a) je uvijek protiv Thimina (T), GUANINE (D) protiv citozina (D) protiv citozina (D).
Nukleotidi su međusobno povezani ne slučajno, već selektivno. Sposobnost biračkog adenina s time i Guaninom sa citozinom naziva se komplementarna. Komplementarna interakcija određenih nukleotida objašnjava se osobitostima prostornog uređenja atoma u svojim molekulama koji im omogućavaju zatvaranje i formiranje n-obveznica. U lancu polinukleotida, susjedni nukleotidi su međusobno povezani šećerom (deoksirilozom) i ostatkom fosforne kiseline. RNA kao i DNK je polimer čiji su monomeri nukleotidi. Dušine osnove tri nukleotida isto su kao dio DNK (A, G, C) - četvrti - uracil (y) prisutan je u molekuli RNA umjesto oma. Nukleotidi RNA razlikuju se od DNK nukleotida i na strukturi ugljikohidrata uključene u njihov sastav (riboza umjesto Dysoxyriboza).
U lancu RNA nukleotida kombiniraju se formiranjem kovalentnih obveznica između riboze jednog nukleotida i ostatka fosforne kiseline drugog. Struktura se razlikuje dva lanca RNA. Dva lanca RNAS su čuvari genetskih informacija u nizu virusa, t.E. Oni obavljaju funkcije kromosoma. Jedan lanac RNA prebaci informacije o strukturi proteina od hromosoma do mjesta njihove sinteze i sudjeluje u sintezi proteina.
Postoji nekoliko vrsta jednog lanca RNA. Njihova imena su zbog funkcije ili lokacije u ćeliji. Većina citoplazme RNA (do 80-90%) je ribosomalna RNA (RRNA) sadržana u ribosomima. Molekuli RRNA relativno su mali i sastoje se u prosjeku 10 nukleotida. Druga vrsta RNA (IRNN) noseći informacije o nizu aminokiselina u proteinima koji se sintetizira u ribosome. Veličina ovih RNA ovisi o dužini DNK odjeljka na kojem su sintetizirani. Transport RNA izvrši nekoliko funkcija. Oni isporučuju aminokiseline na mjesto sinteze proteina ", prepoznaju" (na principu komplementarnosti) trostruka i RNA koja odgovara prijenosnom aminokiselinu izvedi tačnu orijentaciju aminokiseline na ribosomu.
Masti i lipidi

Masti su jedinjenja masnih visokih molekularnih utega i trubatomičnih alkoholnih glicerina. Masnoće se ne rastvaraju u vodi - oni su hidrofobični. U CAGE su uvijek ostale složene hidrofobne masti tvari u kavezu, nazivaju lipoidi.Jedna od glavnih funkcija masti je energija. Za vrijeme dijeljenja 1 g. Masti do S2 i N2Otprilike velika količina energije je izuzeta - 38,9 KJ (~ 9.3 kcal). Sadržaj masti u ćeliji se kreće u rasponu od 5-15% mase suhe materije. U ćelijama živahnog tkiva, količina masti se povećava na 90%. Glavna funkcija masti u životinjskoj (i dijelom - povrće) svijet - čarapa.
Sa punom oksidom od 1 g masti (u ugljični dioksid i vodu), razlikuje se oko 9 kcal energije. (1000 CACALO (CAL, CAL) - incidentna jedinica količine posla i energije jednaka količini topline potrebna za grijanje 1 ml vode na 1 ° C sa standardnim atmosferskim pritiskom od 101.325 kPa-1 kcal = 4,19 KJ). Kada oksidirajući (u tijelu), 1 g proteina ili ugljikohidrata izdvaja se samo oko 4 kcal / g. Na raznim vodenim organizmima - od jednoćelijskih dijatoma algi do džinovskih morskih pasa - masnoća traži "plovak", smanjujući prosječnu gustoću tijela. Gustina životinjske masti je oko 0,91-0,95 g / cm³. Gustina kosti kralježaka blizu 1,7-1.8 g / cm³, a prosječna gustina većine ostalih tkiva je blizu 1 g / cm³. Jasno je da masnoća treba prilično puno za "ravnotežu" teškim kosturu.
Masti i lipidi obavljaju građevinsku funkciju: oni su dio ćelijskih membrana. Zbog loše termalne provodljivosti masnoća može zaštititi funkciju. U nekim životinjama (pečati, kitovi) odgođen je u potkožnom masnom tkivu, formirajući sloj s debljinom do 1 m. Formiranje nekih lipoida prethodi sintezi više hormona. Stoga su ove tvari svojstvene funkcije reguliranja metaboličkih procesa.